Všetko o osmie

Osmium - vzácny kov, patrí do skupiny platiny. Objavili ho v Anglicku ako výsledok pokusov o reakcii platiny. Názov osmium je uvedený v gréčtine a v preklade znamená "vôňa". Aký je tento ušľachtilý kov? Aké sú jeho vlastnosti a aké je jeho využitie?

História
K objavu tohto prvku došlo náhodou v roku 1803 anglickými chemikmi Smithson Tennant a William H. Wollastan. V dôsledku pokusov o reakcii platiny na zmes kyselín (sírovej a dusičnej) sa vo výslednej zrazenine vyvinula nepríjemná aróma, pripomínajúca smrad chlóru a hnilú reďkovku. Podobné experimenty vykonali Colle-Descoti, Antoine de Fourcoy a Vauquelin vo Francúzsku. V dôsledku svojho výskumu našli neznámu látku aj v nerozpustnom sedimente z platiny.



Vtedy neznáma látka dostala názov kuriatko, ale pokusy Britov dokázali, že ide o dve podobné látky – irídium a osmium.
Objav týchto chemických prvkov bol predložený Kráľovskej spoločnosti v Londýne Tennantovým písomným oznámením z 21. júna 1804. V periodickej tabuľke chemických prvkov Mendelejeva sa kov nachádza pod poradovým číslom 76. Kov sa nevyskytuje vo svojej čistej forme v zrnkách, preto je jeho chemický vzorec prezentovaný v rozpustenej forme.


Prvok sa získava z druhotných surovín v dôsledku jeho oddelenia od irídiových, platinových, platino-paládiových rúd alebo medených a niklových rúd. Ročná produkcia celého prvku vo svete nepresahuje veľkosť 1 tony.


Miesto narodenia
Najväčšie svetové ložiská stoja za povšimnutie také zóny ako napr Uralské pohorie a Sibír v Rusku, severnom štáte Aljaška a západný štát Kalifornia v Amerike, Kanada v Severnej Amerike, Kolumbia v Južnej Amerike a niektoré juhoafrických krajinách, Austrália, Ostrov Tasmánia... V súčasnosti sa uvažuje o významnom ložisku osmia Bushwell Complex v Južnej Afrike, tam sa ťaží väčšina látky. Ak vezmeme do úvahy, že najväčšie ložiská kovu sú v Južnej Afrike, svetové ceny tohto kovu vzácnych zemín sú dosť vysoké. Kazachstan je považovaný za jediného veľkého vývozcu osmia-187 na svete. Hoci Čína má zásoby platinovej rudy, nemá významné množstvo osmia.


Látka je skladovaná v práškovej forme a keďže sa netopí vo forme kryštálov, nie je možné na ňu pre jej fyzikálne vlastnosti nalepiť pečiatku. Na výrobu ingotov z tohto kovu sa používa ohrev elektrónovým lúčom alebo oblúkový ohrev z prášku, tiež ohrev v tégliku.


Vlastnosti
Osmium vyzerá ako striebristo modrastý kov. Je to jeden z najhustejších prvkov, jeho hustota je 22 600 kilogramov na meter kubický, no zároveň je hmota dosť krehká, ľahko sa láme a drobí. Má vysokú špecifickú hmotnosť a je schopný svietiť aj pri pomerne vysokých teplotných vplyvoch. Pre jeho parametre a výraznú teplotu tavenia je náročné ho opracovať. V prírode existuje vo forme siedmich izotopov, z ktorých šesť sa považuje za stabilné, sú to osmium-184, osmium-187, osmium-188, osmium-189, osmium-190 a osmium-192. V laboratóriu sa získali izotopy rádioaktívnych kovov s hmotnostnými číslami od 162 do 197 a niektoré jadrové izoméry sa získali aj umelo.
Osmium svojimi vlastnosťami nepriaznivo ovplyvňuje všetky živé organizmy.

Takmer všetky zlúčeniny s týmto kovom spôsobujú poškodenie vnútorných orgánov, poruchy zraku a sluchu. V prípade otravy parami osmia môže dôjsť k nezvratným poruchám v tele a smrti. Vedci uskutočnili experimenty na zvieratách, ktorých výsledkom bol rýchly rozvoj anémie, nedostatok normálnej funkcie pľúc. Dospelo sa k záveru, že ide o rýchlo sa rozvíjajúci edém. Oxid osmičelý, ktorý sa používa v medicíne, je veľmi žieravá látka. Má ten najnepríjemnejší zápach na svete. Pri otravách koža trpí, mení farbu na zelenú alebo čiernu, často sprevádzané vredmi a prasklinami, ktorých liečenie bude trvať veľmi dlho.

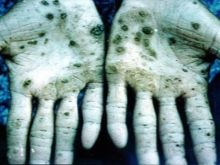

Najviac ohrození sú zamestnanci výrobných prevádzok, ktorí podľa všetkých bezpečnostných noriem pracujú len v respirátoroch a špeciálnom oblečení. Všetky nádoby obsahujúce oxid osmičelý sú zapečatené a skladované v súlade s pravidlami. Na získanie minerálov nevyanskitu sa platina premieňa na roztok pomocou aqua regia. Potom sa výsledná zrazenina vystaví pôsobeniu zinku v 8-násobnom množstve - takáto zliatina sa pomerne ľahko premení na práškový stav, ktorý sa potom taví s peroxidom bárnatého. Ďalším stupňom je spracovanie výslednej hmoty s aqua regia, destilácia cez aparatúru na oddeľovanie oxidu osmičelého.

Pôsobením na látku alkalickým roztokom sa získa soľ. Ovplyvnený je fyziologický roztok hyposulfit, v dôsledku čoho sa kov pomocou chloridu amónneho vyzráža už vo forme Fremyho soli. Zrazenina sa premyje, filtruje a kalcinuje. Výsledkom všetkých týchto akcií je hubovité osmium. Následne sa čistí kyselinami, redukuje v elektrickej peci pod prúdom vodíka a ochladí. Takže získať vzorky osmia až do 99,9%.


Chemický
Vlastnosti tohto prvku sú z hľadiska chémie úžasné. Najzákladnejšie z nich sú nasledujúce.
- Osmium vôbec nereaguje s alkáliami a kyselinami. V reakcii s alkalickými taveninami vytvára vo vode rozpustné osmáty. Interakcia so zmesou kyseliny dusičnej a chlorovodíkovej dáva extrémne pomalú reakciu.
- Veľmi toxický, dokonca aj v mikroskopických dávkach. Zvlášť toxický je oxid osmiitý, ktorý sa uvoľňuje z platiny.
- Nie je možné určiť bod varu kovu, pretože je obzvlášť žiaruvzdorný.
- Kov v prášku ľahko vstupuje do zahrievacej reakcie s takými látkami: čistý kyslík, halogény, kyselina sírová alebo dusičná.
- V rôznych zlúčeninách sa získajú oxidové čísla od -2 do +8. Najbežnejšie sú +2, +3, +4 a +8.
- Schopný vytvárať klastrové zlúčeniny.
- Hlavné minerály súvisia s tuhými roztokmi a sú zastúpené zliatinami irídia s osmiom - sú to sysertskit a nevyanskit. Okrem toho má syserskit iný názov - dúhové osmium a nevyanskit - osmózne irídium.

Fyzické
Hustota osmium je približne 22,61 gramov na centimeter kubický. Kryštály majú krásny striebristý lesk s rôznymi odtieňmi od šedej po modrú. V ingotoch sa objavuje tmavomodrá farba, v prášku je fialová. Celý kov má strieborný lesk. Toxicita prvku bráni jeho použitiu v klenotníckom priemysle. Hlavné fyzikálne vlastnosti sú nasledovné.
- Teplota topenia tohto prvku je pomerne vysoká, topenie je možné pri teplotách nad 3000 stupňov Celzia.
- Kov nemá magnetické vlastnosti.
- Úžasná pevnosť. Zliatiny s prídavkom tohto kovu získavajú zvýšenú odolnosť proti opotrebovaniu, trvanlivosť, odolnosť proti korózii a odolnosť voči mechanickému namáhaniu.
- Bod varu je 5012 ºC.
- Mohsova tvrdosť je 7.
- Tvrdosť podľa Vickersa je 3-4 GPa.

Aplikácie
Vzhľadom na značné náklady na samotný prvok sa tento kov zriedka používa v masovej priemyselnej výrobe. Osmium sa používa najmä v chemickom priemysle, kde sa používa ako katalyzátor. V niektorých liekoch sa používa oxid osmičelý. V laboratórnych rozboroch sa používa na farbenie živých tkanív, zabezpečuje zachovanie bunkovej štruktúry.
V leteckom priemysle sa používa osmium v elektronickom vybavení zariadení pre leteckú a raketovú techniku, ako aj pri výrobe jadrové zbrane. Kvôli nedostatku magnetických vlastností, kov sa používa pri výrobe značkových hodiniek ako napríklad Rolex. Zliatina osmia s platinou sa používa, keď vytváranie chirurgických implantátov Sú to kardiostimulátory alebo pľúcne chlopne.
Okrem toho sa osmium používa v mikroskopii a na vytváranie vysoko presných prístrojov.



Zaujímavosti
- Pod tlakom asi 770 GPa v osmie interagujú elektróny vo vnútorných orbitáloch, štruktúra látky zostáva nezmenená.
- Osmium v horninách obsahuje pol percenta celkovej hmoty rudných ložísk.
- Kvôli vysokej hustote vzhľad a skutočná hmotnosť kovu sa značne líšia. Takže 0,5 litrová plastová fľaša naplnená týmto kovovým práškom bude ťažšia ako 10 litrové vedro naplnené vodou.
- Tento kov je v piatich najviac nákladné.
- Cena trojitej unce osmia je obchodným tajomstvom, v otvorených zdrojoch nájdete približnú cenu za 1 gram látky.
- Kvôli žiaruvzdornosti osmia zaznamenané v histórii elektrickej lampy. Vedec K. Auer von Welsbach z Nemecka navrhol nahradiť uhlíkové vlákno v žiarovke vláknom z osmia. Žiarovky sa ukázali ako 3-krát menej energeticky náročné a osvetlenie sa výrazne zlepšilo. Pravda, čoskoro bol nahradený bežnejším tantalom, ktorý bol naopak nahradený volfrámom.
- Podobná situácia nastala so vzácnym kovom pri výrobe čpavku. Metóda syntézy amoniaku, ktorá sa používa dodnes, vyvinutá v roku 1908 chemikom Fritzom Haberom z Nemecka, je nemožná bez použitia katalyzátorov.Katalyzátory používané v tom čase spočiatku vykazovali svoje vlastnosti iba za prítomnosti výrazných teplotných podmienok a nemali vysokú účinnosť, takže hľadanie náhrady bolo veľmi naliehavé. Vedci z laboratória Vyššej technickej školy v Karlsruhe navrhli použiť ako katalytický prvok jemne atomizované osmium. Výsledky testov potvrdili, že tento nápad stojí za to, katalytická teplota klesla o viac ako 100 ºC a výrazne sa zvýšilo uvoľňovanie amoniaku. Je pravda, že v budúcnosti odmietli osmium, ale pomohol pri riešení takého dôležitého problému.

Osmium a iné vzácne a jedinečné kovy hrajú významnú úlohu v rôznych priemyselných odvetviach... Aj pri všetkej svojej toxicite zachraňuje životy a zdravie ľudí.
Viac informácií o osmie nájdete v nasledujúcom videu.








